Un team guidato dall’Ifac-Cnr di Firenze, che comprende l’Ifc-Cnr e l’Università di Firenze, ha messo a punto un’innovativa metodica per caricare con nanoparticelle d’oro le cellule immunitarie, che diventano così in grado di localizzare le patologie neoplastiche, distruggendole con una sorta di ‘bomba’. La tecnica è stata sperimentata in colture cellulari e modelli biologici e illustrata su Advanced Functional Materials
Veicolare agenti diagnostici e terapeutici nell’organismo umano sfruttando una delle caratteristiche più insidiose delle cellule tumorali, la loro abilità di asservire il sistema immunitario alla propria proliferazione e diffusione. È quanto sono riusciti a realizzare ricercatori del Consiglio nazionale delle ricerche dell’Istituto di fisica applicata (Ifac-Cnr), in collaborazione con colleghi dell’Istituto di fisiologia clinica (Ifc-Cnr) e del Dipartimento di scienze biomediche sperimentali e cliniche dell’Università di Firenze. I risultati dello studio sono stati pubblicati sulla rivista Advanced Functional Materials.
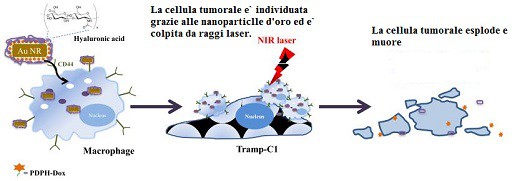
“L’obiettivo terapeutico è quello di intercettare quelle cellule immunitarie, come i macrofagi, che accorrono in soccorso alle cellule tumorali, estrarle dal paziente e caricarle di nano-particelle d’oro affinché funzionino da nano-traccianti e ‘nano-bombe’”, spiega Fulvio Ratto dell’Ifac-Cnr, primo autore del lavoro. “Quindi le cellule così trattate verranno re-iniettate nel sangue del paziente, per fare sì che proseguano il proprio cammino verso l’ambiente tumorale. Infine, le nanoparticelle che esse trasportano verranno attivate con luce laser, come un detonatore da remoto, per indurre effetti deflagranti all’interno del tumore”.
I nanocilindri d’oro sviluppati dall’équipe guidata dall’Ifac-Cnr sono capaci di emettere ultrasuoni oppure di surriscaldarsi a seconda del laser impiegato. “Abbiamo verificato che i macrofagi caricati con centinaia di migliaia di nanoparticelle mantengono molte loro funzioni biologiche, tra cui soprattutto la predisposizione a migrare verso l’ambiente tumorale”, specifica Ratto. “Inoltre, mediante uno strumento simile ad un ecografo clinico”, prosegue Luca Menichetti, ricercatore di Ifc-Cnr, “è stato possibile individuare e localizzare con elevata precisione le nanoparticelle nei tessuti biologici sede del tumore. A questo punto, illuminando la regione con un laser a diodo di bassa potenza, è possibile provocarne in modo controllato il surriscaldamento e determinare un danno irreversibile alle cellule tumorali”.
Gli esperimenti condotti finora in colture cellulari e modelli biologici hanno dimostrato la fattibilità di questo approccio, aprendo nuovi scenari terapeutici nella battaglia contro il cancro. “La metodica prospetta una medicina veramente personalizzata, basata sulle cellule immunitarie che il paziente sviluppa in risposta allo specifico tumore”, conclude Roberto Pini, direttore dell’Ifac-Cnr e coordinatore del gruppo di ricerca. “La strada è però ancora lunga: sarà infatti necessaria una complessa fase di test preclinici, prima di poter applicare questa metodica sull’uomo. Tuttavia, riteniamo che le sinergie tra nanotecnologie, fotonica e biologia cellulare – le discipline alla base di questo studio – abbiano grandi potenzialità per fornire uno strumento efficiente e versatile per la diagnosi e la cura di molti tumori”.